1998年に受精卵からヒト胚性幹細胞(以降、ヒトES細胞という.)が樹立され、さらに2007年に京都大学iPS研究所山中教授らによってヒトの体性幹細胞からiPS細胞が樹立されました. ヒトES細胞及びiPS細胞は、高い増殖能と固体を形成する全ての細胞種へ分化可能な幹細胞で、新たな疾患の治療法となる多能性幹細胞です.
1. 従来の細胞移植療法に用いられる細胞
患者さんの組織にある組織や線維芽細胞を大量培養増殖し、治療局所部位
に移植するものです.
(例) 自家培養軟骨細胞、自家培養角膜細胞、筋芽細胞増殖ハートシーが商品化されました.
2. 組織幹細胞
組織幹細胞の特徴として、各臓器・組織に存在する自己複製能と所属組織の構成細胞種への分化能を有し、
それが属している組織または臓器構成細胞種への限られた分化能しか示さない幹細胞です(多能性を示さない).
組織幹細胞は、臨床応用に優れ現在、患者様の組織や臓器にわずかに存在する組織幹細胞を大量培養し患者様に移植する
治療法が、国内において医学研究また国外では治験が実施されています.
(例)造血幹細胞(適応症:白血病、悪性リンパ腫)
ヒト同種骨髄由来間葉系幹細胞(適応症:移植片対宿病)
神経組織幹細胞(適応症:ドライ型加齢性黄斑変性症〈眼内〉等、国外で治験実施中)
ヒト同種脂肪組織間葉系幹細胞(適応症:慢性虚血性心筋症等、国外で治験実施中)
3. 多能性幹細胞
無限の増殖能と全身の細胞種への多分化能を有し、多能性幹細胞から分化誘導された特定細胞種を移植することによって
臓器機能の回復を図る細胞療法の実現化が図られています.
・ヒトES幹細胞
ヒト受精卵胎盤の一部から樹立された幹細胞です. 細胞種への多分化能を保持した未分化状態を維持することが可能
で、がん細胞と異なり正常な遺伝子を保持したまま培養系で無限に蔵宿できる特徴を有しています. 再生医療の実現
化のため、ES幹細胞から特定細胞種への分化誘導開発と増殖技術の確立を急ぐ必要があり、特に分化誘導開発には
ケミカルバイオロジー(増殖因子、遺伝子組換え等の分化誘導手段)が必要な開発手段と考えられています.
(例) ヒトES幹細胞株の分化誘導を介して得られた膵臓内胚葉細胞
(適応症:タイプI型糖尿病〈膵臓β細胞の再生〉、海外で治験中)
〈Technical Term〉
フィーダー細胞、未分化状態維持機構、分化誘導剤(増殖因子、細胞外マトリックス、遺伝子操作)
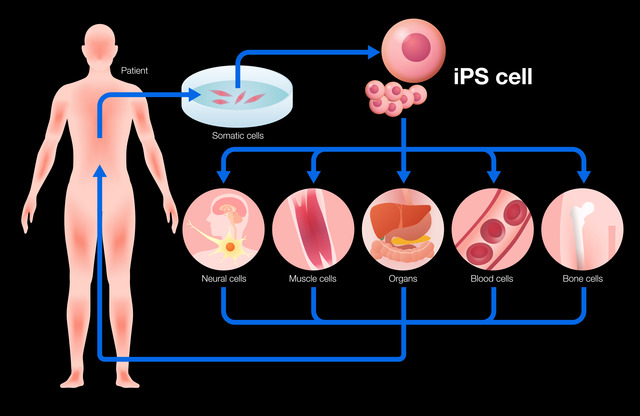
・ヒトiPS細胞
ヒト線維芽細胞にレトロウイルスを用いた山中4因子の導入により、ヒトES細胞と同じ多能性を有するヒトiPS細胞
(Nanog-iPS細胞)が得られました. また米国では異なる4因子の組合せ(OCT4, SOX2, NANOG, LIN28)をヒト線維芽
細胞に導入し、同様にヒトiPS細胞が得られています (Yu, J., et Al.: Science, 318: 1917-20, 2007).
ヒトiPS細胞の利点は、自家体細胞から樹立されるため拒絶反応のない移植療法の開発を可能にしました.
また、患者体細胞からiPS細胞を樹立し、培養系で遺伝し組換えにて原因遺伝子を修復する新たな細胞療法の開発が期
待されています. しかし、ヒトiPS細胞とヒトSE細胞の比較に関し、未だ医学的な研究の結論は得られていません.
iPS細胞を用いた国内開発状況:臨床研究は行われていますが、GCP及びGCTPに対応した治験は未だ準備段階です.
〈Technical Term〉
体細胞、リプログラミング、山中4因子、細胞融合、疾患特異的iPS細胞、特定細胞種への分化誘導、
再生医療用iPS細胞バンク、遺伝子治療との組合せた細胞療法の開発研究